其实很多同学没明白实验在化学学习及高考中有举足轻重的作用,所以导致失掉很多不该丢的分数,但实验题在高考理科综合中占有很大的分值。以下8条关于高中化学实验的超级总结,一定助你在大题上少丢分!
一
化学实验操作中的七原则
掌握下列七个有关操作顺序的原则,就可以正确解答“实验程序判断题”。
1.“从下往上”原则。
以Cl2实验室制法为例,装配发生装置顺序是:
放好铁架台→摆好酒精灯→根据酒精灯位置固定好铁圈→石棉网→固定好圆底烧瓶。
2.“从左到右”原则。装配复杂装置遵循从左到右顺序。
如上装置装配顺序为:发生装置→集气瓶→烧杯。
3.先“塞”后“定”原则。带导管的塞子在烧瓶固定前塞好,以免烧瓶固定后因不宜用力而塞不紧或因用力过猛而损坏仪器。
4.“固体先放”原则。上例中,烧瓶内试剂MnO2应在烧瓶固定前装入,以免固体放入时损坏烧瓶。总之固体试剂应在固定前加入相应容器中。
5.“液体后加”原则。液体药品在烧瓶固定后加入。如上例浓盐酸应在烧瓶固定后在分液漏斗中缓慢加入。
6.先验气密性(装入药口前进行)原则。
7.后点酒精灯(所有装置装完后再点酒精灯)原则。
二
化学实验中温度计的使用
分哪三种情况以及哪些实验需要温度计?
1.测反应混合物的温度:这种类型的实验需要测出反应混合物的准确温度,因此,应将温度计插入混合物中间。
①测物质溶解度。
②实验室制乙烯。
2.测蒸气的温度:这种类型的实验,多用于测量物质的沸点,由于液体在沸腾时,液体和蒸气的温度相同,所以只要测蒸气的温度。
①实验室蒸馏石油。
②测定乙醇的沸点。
3.测水浴温度:这种类型的实验,往往只要使反应物的温度保持相对稳定,所以利用水浴加热,温度计则插入水浴中。
①温度对反应速率影响的反应。
②苯的硝化反应。
三
常见的需要塞入棉花的实验
需要塞入少量棉花的实验:
加热KMnO4制氧气
制乙炔和收集NH3
其作用分别是:防止KMnO4粉末进入导管;
防止实验中产生的泡沫涌入导管;
防止氨气与空气对流,以缩短收集NH3的时间。
四
常见物质分离提纯的10种方法
1.结晶和重结晶:利用物质在溶液中溶解度随温度变化较大,如NaCl,KNO3。
2.蒸馏冷却法:在沸点上差值大。乙醇中(水):加入新制的CaO吸收大部分水再蒸馏。
3.过滤法:溶与不溶。
4.升华法:SiO2(I2)。
5.萃取法:如用CCl4来萃取I2水中的I2。
6.溶解法:Fe粉(Al粉):溶解在过量的NaOH溶液里过滤分离。
7.增加法:把杂质转化成所需要的物质:CO2(CO):通过热的CuO;
CO2(SO2):通过NaHCO3溶液。
8.吸收法:除去混合气体中的气体杂质,气体杂质必须被药品吸收;
N2(O2):将混合气体通过铜网吸收O2。
9.转化法:两种物质难以直接分离,加药品变得容易分离,然后再还原回去:Al(OH)3,Fe(OH)3:先加NaOH溶液把Al(OH)3溶解,过滤,除去Fe(OH)3,再加酸让NaAlO2转化成A1(OH)3。
五
常用的去除杂质的方法10种
1.杂质转化法:欲除去苯中的苯酚,可加入氢氧化钠,使苯酚转化为酚钠,利用酚钠易溶于水,使之与苯分开。欲除去Na2CO3中的NaHCO3可用加热的方法。
2.吸收洗涤法:欲除去二氧化碳中混有的少量氯化氢和水,可使混合气体先通过饱和碳酸氢钠的溶液后,再通过浓硫酸。
3.沉淀过滤法:欲除去硫酸亚铁溶液中混有的少量硫酸铜,加入过量铁粉,待充分反应后,过滤除去不溶物,达到目的。
4.加热升华法:欲除去碘中的沙子,可用此法。
5.溶剂萃取法:欲除去水中含有的少量溴,可用此法。
6.溶液结晶法(结晶和重结晶):欲除去硝酸钠溶液中少量的氯化钠,可利用二者的溶解度不同,降低溶液温度,使硝酸钠结晶析出,得到硝酸钠纯晶。
7.分馏蒸馏法:欲除去乙醚中少量的酒精,可采用多次蒸馏的方法。
8.分液法:欲将密度不同且又互不相溶的液体混合物分离,可采用此法,如将苯和水分离。
9.渗析法:欲除去胶体中的离子,可采用此法。如除去氢氧化铁胶体中的氯离子。
10.综合法:欲除去某物质中的杂质,可采用以上各种方法或多种方法综合运用。
六
化学实验基本操作中的“不”15例
1.实验室里的药品,不能用手接触;不要鼻子凑到容器口去闻气体的气味,更不能尝结晶的味道。
2.做完实验,用剩的药品不得抛弃,也不要放回原瓶(活泼金属钠、钾等例外)。
3.取用液体药品时,把瓶塞打开不要正放在桌面上;瓶上的标签应向着手心,不应向下;放回原处时标签不应向里。
4.如果皮肤上不慎洒上浓H2SO4,不得先用水洗,应根据情况迅速用布擦去,再用水冲洗;若眼睛里溅进了酸或碱,切不可用手揉眼,应及时想办法处理。
5.称量药品时,不能把称量物直接放在托盘上;也不能把称量物放在右盘上;加法码时不要用手去拿。
6.用滴管添加液体时,不要把滴管伸入量筒(试管)或接触筒壁(试管壁)。
7.向酒精灯里添加酒精时,不得超过酒精灯容积的2/3,也不得少于容积的1/3。
8.不得用燃着的酒精灯去对点另一只酒精灯;熄灭时不得用嘴去吹。
9.给物质加热时不得用酒精灯的内焰和焰心。
10.给试管加热时,不要把拇指按在短柄上;切不可使试管口对着自己或旁人;液体的体积一般不要超过试管容积的1/3。
11.给烧瓶加热时不要忘了垫上石棉网。
12.用坩埚或蒸发皿加热完后,不要直接用手拿回,应用坩埚钳夹取。
13.使用玻璃容器加热时,不要使玻璃容器的底部跟灯芯接触,以免容器破裂。烧得很热的玻璃容器,不要用冷水冲洗或放在桌面上,以免破裂。
14.过滤液体时,漏斗里的液体的液面不要高于滤纸的边缘,以免杂质进入滤液。
15.在烧瓶口塞橡皮塞时,切不可把烧瓶放在桌上再使劲塞进塞子,以免压破烧瓶。
七
化学实验中的先与后22例
1.加热试管时,应先均匀加热后局部加热。
2.用排水法收集气体时,先拿出导管后撤酒精灯。
3.制取气体时,先检验气密性后装药品。
4.收集气体时,先排净装置中的空气后再收集。
5.稀释浓硫酸时,烧杯中先装一定量蒸馏水后再沿器壁缓慢注入浓硫酸。
6.点燃H2、CH4、C2H4、C2H2等可燃气体时,先检验纯度再点燃。
7.检验卤化烃分子的卤元素时,在水解后的溶液中先加稀HNO3再加AgNO3溶液。
8.检验NH3(用红色石蕊试纸)、Cl2(用淀粉KI试纸)、H2S[用Pb(Ac)2试纸]等气体时,先用蒸馏水润湿试纸后再与气体接触。
9.做固体药品之间的反应实验时,先单独研碎后再混合。
10.配制FeCl3,SnCl2等易水解的盐溶液时,先溶于少量浓盐酸中,再稀释。
11.中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准掖;先用待测液润洗后再移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点。
12.焰色反应实验时,每做一次,铂丝应先沾上稀盐酸放在火焰上灼烧到无色时,再做下一次实验。
13.用H2还原CuO时,先通H2流,后加热CuO,反应完毕后先撤酒精灯,冷却后再停止通H2。
14.配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用胶头滴管加水至刻度线。
15.安装发生装置时,遵循的原则是:自下而上,先左后右或先下后上,先左后右。
16.浓H2SO4不慎洒到皮肤上,先迅速用布擦干,再用水冲洗,最后再涂上3%一5%的NaHCO3溶液。沾上其他酸时,先水洗,后涂NaHCO3溶液。
17.碱液沾到皮肤上,先水洗后涂硼酸溶液。
18.酸(或碱)流到桌子上,先加NaHCO3溶液(或醋酸)中和,再水洗,最后用布擦。
19.检验蔗糖、淀粉、纤维素是否水解时,先在水解后的溶液中加NaOH溶液中和H2SO4,再加银氨溶液或Cu(OH)2悬浊液。
20.用pH试纸时,先用玻璃棒沾取待测溶液涂到试纸上,再把试纸的颜色跟标准比色卡对比,定出pH。
21.配制和保存Fe2+,Sn2+等易水解、易被空气氧化的盐溶液时;先把蒸馏水煮沸赶走O2,再溶解,并加入少量的相应金属粉末和相应酸。
22.称量药品时,先在盘上各放二张大小,重量相等的纸(腐蚀药品放在烧杯等玻璃器皿),再放药品。加热后的药品,先冷却,后称量。
八
实验中导管和漏斗的位置的放置方法
在许多化学实验中都要用到导管和漏斗,因此,它们在实验装置中的位置正确与否均直接影响到实验的效果,而且在不同的实验中具体要求也不尽相同。下面是结合实验和化学课本中的实验图,作一简要的分析和归纳,希望对大家有帮助。
1.气体发生装置中的导管;在容器内的部分都只能露出橡皮塞少许或与其平行,不然将不利于排气。
2.用排空气法(包括向上和向下)收集气体时,导管都必领伸到集气瓶或试管的底部附近。这样利于排尽集气瓶或试管内的空气,而收集到较纯净的气体。
3.用排水法收集气体时,导管只需要伸到集气瓶或试管的口部。原因是“导管伸入集气瓶和试管的多少都不影响气体的收集”,但两者比较,前者操作方便。
4.进行气体与溶液反应的实验时,导管应伸到所盛溶液容器的中下部。这样利于两者接触,充分反应。
5.点燃H2、CH4等并证明有水生成时,不仅要用大而冷的烧杯,而且导管以伸入烧杯的1/3为宜。若导管伸入烧杯过多,产生的雾滴则会很快气化,结果观察不到水滴。
6.进行一种气体在另一种气体中燃烧的实验时,被点燃的气体的导管应放在盛有另一种气体的集气瓶的中央。不然,若与瓶壁相碰或离得太近,燃烧产生的高温会使集气瓶炸裂。
7.用加热方法制得的物质蒸气,在试管中冷凝并收集时,导管口都必须与试管中液体的液面始终保持一定的距离,以防止液体经导管倒吸到反应器中。
8.若需将HCl、NH3等易溶于水的气体直接通入水中溶解,都必须在导管上倒接一漏斗并使漏斗边沿稍许浸入水面,以避免水被吸入反应器而导致实验失败。
9.洗气瓶中供进气的导管务必插到所盛溶液的中下部,以利杂质气体与溶液充分反应而除尽。供出气的导管则又务必与塞子齐平或稍长一点,以利排气。
10.制H2、CO2、H2S和C2H2等气体时,为方便添加酸液或水,可在容器的塞子上装一长颈漏斗,且务必使漏斗颈插到液面以下,以免漏气。
11.制Cl2、HCl、C2H4气体时,为方便添加酸液,也可以在反应器的塞子上装一漏斗。但由于这些反应都需要加热,所以漏斗颈都必须置于反应液之上,因而都选用分液漏斗。
九
高考冲刺化学综合实验题中这些常考点你得知道
新课标全国卷中,综合实验题一般有知识容量大、命题素材广、考查角度多、综合程度高等特点,通常考查基本仪器的识别与使用,物质的制备、除杂与分离,物质性质的探究或验证,实验现象分析或描述,实验结论与评价,数据处理等。复习备考过程中了解综合实验题的命题特点、掌握其必知考点,可以在考试中起到事半功倍的效果。
一、综合实验题的命题特点
综合实验题,从命题形式看,可以分为物质制备实验题、性质探究实验题、方案设计实验题;从命题素材看,可以分为无机实验题、有机实验题。分析近几年高考试题不难发现,综合实验题命题时注重综合,强调创新,尝试开放,每年均会考查操作、现象、目的或原因;可能会考查计算、实验设计、方案优缺点比较等。
二、综合实验题的必知考点
1.常用仪器的使用及实验基本操作
常用仪器的使用包括仪器的名称、用途、使用方法、注意事项,实验基本操作包括仪器的洗涤、连接与气密性(漏液)检查、溶液的配制和稀释、试剂的取用和保存、试纸的使用、一般常见事故处理、“沉淀”处理三步骤(过滤、洗涤、干燥)等。
2019年新课标全国卷Ⅰ第26题考查水蒸气发生装置中长玻璃管平衡压强的作用和碎瓷片防止暴沸的作用,
2019年新课标全国卷Ⅱ第28题考查溶液配制所需的仪器,
2019年新课标全国卷Ⅲ第26题考查干燥管的名称;
2018年新课标全国卷Ⅱ第28题考查FeCl2溶液的配制,
2018年新课标全国卷Ⅲ第26题考查沉淀的过滤、洗涤。
因此,在复习过程中,要注意对常用仪器的结构、使用等进行系统全面地归纳总结,特别是装置的组合使用,如广口瓶和导管的组合,可以有如下几种用途:①洗气瓶,②集气瓶,③安全瓶,④储气瓶。
2.常见气体的制备
常见气体的制备包括所用试剂名称、用量;仪器的选择、连接;反应原理;除杂、干燥、收集方法;尾气处理等。
2018年新课标全国卷Ⅰ第26题考查氨气的制备,2019年新课标全国卷Ⅱ第28题考查ClO2的制备。
复习过程中,要注意对常见气体的制备实验进行系统全面地归纳总结,特别是装置的变形、改进和创新,如启普发生器的简易装置,防倒吸装置等。
3.常见物质的检验及物质分离提纯的方法
常见物质的检验方法包括根据特征阴、阳离子,特殊物理、化学性质,特定实验事实进行检验;物质分离提纯的方法包括溶解、过滤、洗涤、萃取、分液、蒸馏、分馏、结晶、洗气、渗析、升华等方法。
2019年新课标全国卷Ⅲ第26题考查Fe2+的检验,
2018年新课标全国卷Ⅱ第28题考查Fe2+的检验,
2019年新课标全国卷Ⅰ第26题考查草酸晶体分解产物的检验。
复习过程中,要注意对常见物质的检验进行系统全面地归纳总结,如Fe2+的检验方法有:①KSCN溶液、氯水(或双氧水),此方法的前提是溶液中不含Fe3+,取少量溶液于试管中,先加入几滴KSCN溶液,无明显现象,再滴入氯水(或双氧水),溶液变血红色;
②酸性KMnO4溶液,此方法的前提是溶液中不含Cl-等还原性离子,取少量溶液于试管中,加入几滴酸性高锰酸钾溶液,溶液紫色褪去;
③铁氰化钾溶液,此方法是万能的,取少量溶液于试管中,加入几滴K3[Fe(CN)6]溶液,产生蓝色沉淀。
【典例赏析】某同学在实验室制备氯气并进行一系列相关实验,实验装置如下(夹持仪器已略)。
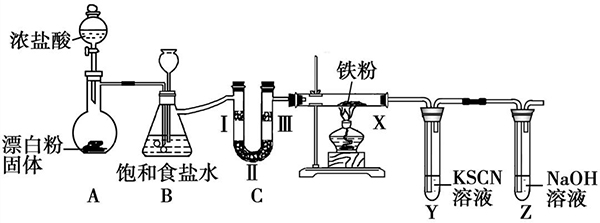
(1)装置A是氯气的发生装置,反应的化学方程式为。
(2)装置B的作用是、。
(3)装置C的实验目的是验证氯气是否具有漂白性,Ⅱ处放入的物质为,实验中观察到Ⅰ、Ⅲ处的有色布条的现象为。
(4)装置X为氯化铁的制备装置。已知:氯化铁易溶于水,熔、沸点低,受热易变为气态,而遇冷又易变为固态。
①试管Y中的现象是,试管Z中氢氧化钠溶液的作用(用离子方程式表示)。
②该同学猜测铁与氯气反应可能还会生成氯化亚铁,为了探究生成物中是否含有氯化亚铁(假设铁已完全反应),请你设计实验方案:取少量X中固体样品于试管中,用适量的蒸馏水溶解,。
【解析】本题考查的内容包括氯气的制备及性质实验、化学实验方案的设计。
(1)装置A为Ca(ClO)2和浓盐酸反应制取氯气的装置。
(2)制备的氯气中含有杂质HCl、水蒸气,装置B的作用为除去HCl,同时起到安全瓶的作用。
(3)氯气能使湿润的有色布条褪色,而不能使干燥有色布条褪色,故Ⅱ处物质应能干燥氯气,选用无水氯化钙。
(4)①X中生成的FeCl3受热气化,进入试管Y中,Y中溶液变为血红色。试管Z中NaOH溶液的作用是吸收氯气尾气,防止污染大气,离子方程式为:Cl2+2OH-ClO-+ Cl-+H2O。
②用铁氰化钾溶液检验Fe2+。
【答案】(1)Ca(ClO)2+4HCl(浓)CaCl2+2Cl2↑+2H2O
(2)除去Cl2中的HCl安全瓶(防止倒吸)
(3)无水CaCl2Ⅰ处有色布条褪色,Ⅲ处有色布条不褪色
(4)①溶液变为血红色Cl2+2OH-ClO-+ Cl-+H2O
②滴入几滴铁氰化钾溶液,若产生蓝色沉淀,则含有Fe2+
本文来自:逍遥右脑记忆 http://www.jiyifa.com/gaokao/1309902.html
相关阅读:高考机器人数学败给文科生 研发人-它读不懂题
