在相同能量的原子轨道上,电子的排布将尽可能占据不同的轨道,而且自旋方向相同,即为洪特规则,又称为最多轨道原理。
一般:电子总是尽先自旋平行地分占不同轨道。如:
碳原子的轨道表示是:
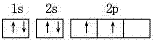 ,而不是
,而不是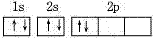
特别提醒:等价轨道全空(p0、d0、f0)和全满时(p6、d10、f14)的结构,也具有较低能量和较大的稳定性。像铁离子Fe3+(3d5)和亚铁离子Fe2+(3d6)对比看,从3d6→3d5才稳定,这和亚铁离子不稳定易被氧化的事实相符合。根据洪特规则铬的电子排布式应为 1s22s22p63s23p63d54s1。
本文来自:逍遥右脑记忆 http://www.jiyifa.com/gaozhong/669952.html
相关阅读:醛酮的加成反应



