就是表示出反应物中原子或离子间的电子转移的方向和数目。
表示方法:
(1)双线桥法:此法不仅能表示出电子转移的方向和总数,还能表示出元素化合价升降和氧化、还原关系。双线桥的箭头始于反应物有关元素的原子或离子,箭头指向发生化合价变化后生成物中对应元素的原子或离子或原子团。如:
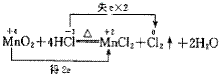
注:箭头表示指向;标“得或失”;箭头表示反应前后变化,不表示电子转移方向
(2)单线桥法:在氧化还原反应中,有电子发生转移(得失或偏移),也就是在反应物中有元素电子发生得失或偏移,这时用一条带箭头的曲线从失去电子的元素指向得到电子的元素,并在“桥”上标出转移的电子数,这种表示方法叫单线桥法。 如:

注:箭头指向;不标“得或失”
双线桥法步骤:
(1)标变价:明确标出所有发生氧化还原反应的元素的化合价,不变价的元素不标化合价。
(2)连双线:将标化合价的同一元素用直线加箭头从反应物指向生成物(注意:箭头的起止要求元素对元素)
(3)标得失:
①标电子转移或偏离数:明确标出得失电子数,格式为“得/失发生氧化还原反应原子个数×单位原子得失电子数”
②标化合价变化:一律标出化合价的变化,只有“化合价升高”“化合价降低”这两种写法,不可写为“升价”“降价”等
③标出元素反应类型:一律标出元素所发生的反应,“被氧化”或“被还原”,其余写法均不正确
④检查得失电子守恒:检查得失电子数是否相等,如不相等则重新分析。
单线桥法步骤:
(1)标价态:明确标明发生氧化还原反应的元素的化合价
(2)连单线:连接方程式左边的氧化剂与还原剂,箭头一律指向氧化剂
(3)不注得失:标出转移的电子的总数,这里不用像双线桥那样,仅需直接标出电子总数
相关高中化学知识点:氧化还原反应的计算
氧化还原反应的计算:
(1)比较典型的计算有:求氧化剂、还原剂物质的量之比或质量比,计算参加反应的氧化剂货还原剂的量,确定反应前后某一元素的价态变化等。
(2)计算的依据是:氧化剂得电子数等于还原剂失电子数,列出守恒关系式求解。
氧化还原反应的基本规律:
1.守恒规律
氧化还原反应中有物质失电子必有物质得电子,且失电子总数等于得电子总数。或者说氧化还原反应中,有元素化合价升高必有元素化合价降低,且化合价升高总数必等于降低总数。有关得失电子守恒(化合价守恒)的规律有如下应用:
(1)求某一反应中被氧化与被还原的元素原子个数之比,或求氧化剂与还原剂的物质的量之比及氧化产物与还原产物的物质的量之比。
(2)配平氧化还原反应方程式。
(3)进行有关氧化还原反应的计算:
2.强弱规律
较强氧化性的氧化剂跟较强还原性的还原剂反应,生成弱还原性的还原产物和弱氧化性的氧化产物。应用:在适宜条件下,用氧化性较强的物质制备氧化性较弱的物质,或用还原性较强的物质制备还原性较弱的物质,也可用于比较物质间氧化性或还原性的强弱。
3.价态规律
元素处于最高价,只有氧化性;元素处于最低价,只有还原性;元素处于中间价态,既有氧化性又有还原性,但主要表现一种性质。物质若含有多种元素,其性质是这些元素性质的综合体现。
4.转化规律
氧化还原反应中,以元素相邻价态之间的转化最容易;不同价态的同种元素之间发生反应,元素的化合价只靠近,不交叉;相邻价态的同种元素之间不发生氧化还原反应。如
5.难易规律
越易失去电子的物质,失去后就越难得到电子;越易得到电子的物质,得到后就越难失去电子。一种氧化剂同时和几种还原剂相遇时,还原性最强的优先发生反应;同理,一种还原剂同时与多种氧化剂相遇时,氧化性最强的优先发生反应,如向FeBr2溶液中通入Cl2时,发生离子反应的先后顺序为:
 。
。
本文来自:逍遥右脑记忆 http://www.jiyifa.com/gaozhong/1036709.html
相关阅读:怎样学好高一化学?



